Un nuevo trabajo liderado por la investigadora del CIBERFES Jennifer Mayordomo, en colaboración con investigadores de la Universidad de Castilla la Mancha y el Instituto Investigación Sanitaria Gregorio Marañón y la Universidad Pablo de Olavide de Sevilla, ha descrito por primera vez en ratones cómo el péptido Aβ25-35 altera el funcionamiento del hipocampo impidiendo el aprendizaje y memoria en ratones. Esta pequeña fracción del péptido amiloide actúa de forma similar a los fragmentos mayores y considerados clínicamente más relevantes en la Enfermedad de Alzheimer.
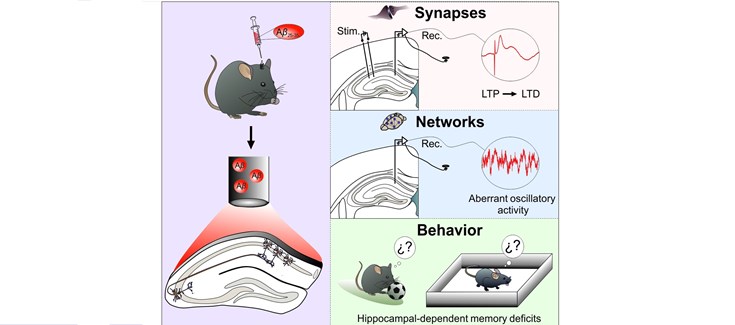
"El fragmento considerado clásicamente como la porción biológicamente activa del péptido-amiloide, de solo 10 aminoácidos situados entre las posiciones 25 y 35 (péptido β-amiloide 25-35, Aβ25-35) induce también una disfunción de las sinapsis hipocampales mediante la generación de LTD en lugar de LTP" explica la investigadora.
Los resultados, publicados en la revista Biology (Q1, I.F. 3.8) muestran, además, que este fragmento amiloide altera la sincronía de la actividad neural de las redes hipocampales. "Ambas alteraciones tienen como resultado profundos déficits de memoria en tareas de aprendizaje que dependen del hipocampo" explica la Dra. Mayordomo.
Según los autores del trabajo el fragmento Aβ25-35 se postula así como un elemento de gran valor para la investigación de la patogénesis relativa a la amiloidosis hipocampal y las etapas preclínicas de la enfermedad de Alzheimer, dada su capacidad para desencadenar los procesos neuropatológicos propios de este trastorno neurodegenerativo.
La investigadora Jennifer Mayordomo, del CIBERFES y del Instituto Investigación Sanitaria Gregorio Marañón, realizó este trabajo como parte de su tesis doctoral junto con otros investigadores del Laboratorio de Neurofisiología y Comportamiento de la Facultad de Medicina de Ciudad Real (CRIB, UCLM) y la División de Neurociencias de la Universidad Pablo de Olavide. Ha contado con financiación del Plan Estatal de Investigación y de la Fundación Tatiana Pérez de Guzmán el Bueno.
Artículo de referencia
Mayordomo-Cava, J.; Iborra-Lázaro, G.; Djebari, S.; Temprano-Carazo, S.; Sánchez-Rodríguez, I.; Jeremic, D.; Gruart, A.; Delgado-García, J.M.; Jiménez-Díaz, L.; Navarro-López, J.D. Impairments of Synaptic Plasticity Induction Threshold and Network Oscillatory Activity in the Hippocampus Underlie Memory Deficits in a Non-Transgenic Mouse Model of Amyloidosis. Biology 2020, 9, 175. https://doi.org/10.3390/biology9070175